ミトコンドリア
ミトコンドリア(mitochondrion、複数形: mitochondria)は真核生物の細胞小器官であり、糸粒体(しりゅうたい)とも呼ばれる。二重の生体膜からなり、独自のDNA(ミトコンドリアDNA=mtDNA)を持ち、分裂、増殖する。mtDNAはATP合成以外の生命現象にも関与する。酸素呼吸(好気呼吸)の場として知られている。また、細胞のアポトーシスにおいても重要な役割を担っている。mtDNAとその遺伝子産物は一部が細胞表面にも局在し突然変異は自然免疫系が特異的に排除[1] する。ヒトにおいては、肝臓、腎臓、筋肉、脳などの代謝の活発な細胞に数百、数千個のミトコンドリアが存在し、細胞質の約40%を占めている。平均では1細胞中に300-400個のミトコンドリアが存在し、全身で体重の10%を占めている[2]。ヤヌスグリーンによって青緑色に染色される。
Contents
構造
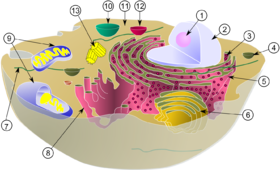
1.内膜 2.外膜 3.クリステ(平板状) 4.マトリックス
ミトコンドリアは、ほとんど全ての真核生物の細胞に含まれる細胞小器官である。直径は0.5 μm程度であるが、形状は生物や細胞の置かれている条件によって多様である。球形、円筒形のものから紐状あるいは網目状のものまであり、長さが10 μmに達するものも珍しくない。1細胞あたりの数は、1つに維持されている細胞もあるが、多い場合では数千個のミトコンドリアが絶えず分裂と融合を繰り返しているものもある。
ミトコンドリアは外膜と内膜という二枚の脂質膜に囲まれており、内膜に囲まれた内側をマトリックス、内膜と外膜に挟まれた空間を膜間腔と呼んでいる。内膜はマトリックスに向かって陥入しクリステ(稜)と呼ばれる特徴的な構造となる。
外膜
外膜の生化学的な組成は細胞膜と同様にタンパク質とリン脂質の重量比がおよそ1:1となっている。外膜にはポリンという膜タンパク質が大量にあり、分子量5000以下の分子が自由に透過できるようなチャネルを形成している。これより大きなタンパク質は自由に出入りすることはなく、ペプチド配列中に移行シグナルが存在している場合にのみ細胞質側から取り込まれる[3]。
外膜の進化的起源は真核生物の細胞内膜系だと考えられ、現在でも小胞体膜と物理的に関係してカルシウムシグナルの伝達や脂質の交換を行っている[4]。
膜間腔
膜間腔はミトコンドリアの外膜と内膜に挟まれた空間であるが、外膜が低分子を自由に透過させる性質であるため、イオンや糖などの組成は細胞質と同等になっている。その一方でタンパク質の組成は細胞質とは異なっており、外膜が破壊されて膜間腔に存在するタンパク質(シトクロムcなど)が細胞質へと漏れ出すとアポトーシスが引き起こされる[5][6]。
内膜
内膜はミトコンドリアの機能的アイデンティティを担っており、酸化的リン酸化に関わる呼吸鎖複合体などの酵素群が規則的に配列している。外膜とは対照的に基本的には不透性で、内外で物質を輸送するためにはそれぞれの物質に対して特異的な輸送体が必要となる。呼吸鎖複合体は内膜をまたぐようにプロトン勾配を形成し、それによって生じる膜電位が物質輸送やATP合成に関与している。そのほかマトリックスへのタンパク質輸送装置やミトコンドリアの分裂・融合に関わるタンパク質群などが存在し、ミトコンドリアを構成する全タンパク質のおよそ2割(150以上)が含まれている。タンパク質とリン脂質の重量比は3:1ほどである。内膜の進化的起源は共生細菌の細胞膜を由来としており、内膜に特徴的なリン脂質カルジオリピンの存在がその証左と考えられている。
一般的に内膜は内側へ向かって陥入しクリステと呼ばれる構造をつくる。これによって内膜の表面積、ひいてはATP合成能の増大に寄与している。外膜と内膜の表面積の比は細胞のATP需要と相関しており、肝臓では5倍ほど、筋細胞ではさらに大きな値となっている[7]。 クリステの形状は生物によって様々であり、平板状、管状、団扇状、などが知られている。多細胞動物や陸上植物ではミトコンドリアの長軸に直交する平板状をしており、教科書などを通じて広く知られている形状である。しかしこれはむしろ特殊なものであり、真核生物全体を見渡すと管状のものが一般的である[8]。
マトリックス
内膜に囲まれた内側がマトリックスであり、TCA回路(クレブス回路・クエン酸回路)やβ酸化などミトコンドリアの代謝機能に関わる酵素群が数多く存在している。ここにはmtDNAが含まれており、ミトコンドリア独自の遺伝情報が保持されている。その遺伝子発現を担うために、リボソーム、tRNA、転写因子や翻訳因子なども存在している。ミトコンドリア全タンパク質の6〜7割が存在しており、非常にタンパク質濃度の高い区画となっている。
機能
ミトコンドリアの主要な機能は電子伝達系による酸化的リン酸化によるATPの産生(ADPのリン酸化)である。細胞のさまざまな活動に必要なエネルギーのほとんどは、直接、あるいは間接的にミトコンドリアからATPの形で供給される。 しかしそれ以外にも多様な機能を持っており、ステロイドやヘムの合成などを含む様々な代謝、カルシウムや鉄の細胞内濃度の調節、細胞周期やアポトーシスの調節などにも大きく関わっているとされる。ただしすべてのミトコンドリアが上記の機能を担っている訳ではなく、あるものはある特定の細胞でのみ機能している。こうした様々な機能には多数の遺伝子が関わっており、それらに変異が自然免疫で排除されないとミトコンドリア病を引き起こすことになる。
エネルギー変換
ATP産生はミトコンドリアの主たる機能であって、これに関わる多くのタンパク質が内膜やマトリックスに存在している。細胞質には解糖系があり、グルコースを代謝することでピルビン酸とNADHを生じる。もし酸素が十分に存在しない場合には解糖系の産物は嫌気呼吸により代謝される。しかしミトコンドリアで酸素を用いてこれらを酸化する好気呼吸を行うことで、嫌気呼吸と比べてはるかに効率よくATPを得ることができる。嫌気性分解では1分子のグルコースから2分子のATPしか得られなかったのが、ミトコンドリアによる好気性分解によって、1分子のグルコースから38分子のATPが合成できるようになった[8]。
ピルビン酸だけでなく、脂肪酸を利用することもできる。植物のミトコンドリアは酸素がなくとも亜硝酸を利用してある程度のATP産生が可能である[9]。
細胞質での解糖系
全ての生物で解糖系はその反応が細胞質基質で起こる。これは解糖系が細胞内小器官が発生する以前から存在する最も原始的な代謝系であることを反映しているのだろう。真核生物では、解糖系でえられた物質(ピルビン酸とNADH)をTCA回路や電子伝達系の反応がおこるミトコンドリアに輸送し、好気呼吸を行う[10]。
ミトコンドリアへの輸送
細胞質の解糖系で生成されたピルビン酸はピルビン酸共輸送体(ピルビン酸/H+)により細胞質からミトコンドリアへ輸送される。同じく細胞質で生成されたNADHはリンゴ酸-アスパラギン酸シャトルによりミトコンドリアへ実質的に輸送される[11]。また、ADPはATP/ADPトランスポーターにより細胞質からミトコンドリアへ輸送される[12]。なお、H2O、O2、CO2、NH3に限ってミトコンドリア内膜を通過することができる。
ピルビン酸の脱炭酸
アセチルCoAは、好気性細胞呼吸の第二段階目であるピルビン酸がピルビン酸デヒドロゲナーゼ複合体により脱炭酸して生成する。この酵素反応はミトコンドリアのマトリックスで起こる。ここで生成したアセチルCoAはクエン酸回路に参加する[13]。
クエン酸回路
解糖系で生じたピルビン酸は内膜を能動輸送によって透過し、マトリックスで酸化され補酵素Aと結合し、二酸化炭素、アセチルCoA、NADHを生じる。アセチルCoAはクエン酸回路へ入る基質である。クエン酸回路の酵素群はほとんどがマトリックスに存在しているが、コハク酸デヒドロゲナーゼ(ユビキノン)だけは例外で内膜の呼吸鎖複合体IIとなっている。クエン酸回路はアセチルCoAを酸化して二酸化炭素を生じ、その過程で3分子のNADHと1分子FADH2、1分子のGTPを生成する。二酸化炭素はミトコンドリア外に排出される。
クエン酸サイクルでは、サイクルの一回転ごとにすべての中間体(例えば、クエン酸、イソクエン酸、α-ケトグルタル酸、コハク酸、フマル酸、リンゴ酸およびオキサロ酢酸)が再生される。 したがって、ミトコンドリアにこれらの中間体のいずれかを追加して加えることは、追加された量がクエン酸サイクル内に保持され、中間体の一つが他方に変換されて順次増加することを意味する。 したがって、それらの中間体のいずれか1つをクエン酸サイクルに加えることは、補充反応(アナプレロティック反応)効果を示し、中間体のいずれかの除去は消費反応(カタプレロティック反応)効果を示す。 これらの補充反応及び消費反応は、クエン酸サイクルの回転でアセチルCoAと結合してクエン酸を形成するために利用可能なオキサロ酢酸の量を増加または減少させる。この回転量がミトコンドリアによるATP製造量と細胞へのATPの提供量の増減を左右することとなる[14]。
電子伝達系
NADHやFADH2のもつ還元力は、内膜にある電子伝達系で数段階を経て酸素に渡される。これら高エネルギー分子は、マトリックスのTCA回路からだけでなく、細胞質の解糖系からも生じる。細胞質で生じた還元等量はマロン酸-アスパラギン酸対向輸送系や、リン酸グリセロールシャトル系を通じて電子伝達系に供給される。内膜の電子伝達系には、NADH脱水素酵素、シトクロームc還元酵素、シトクロームc酸化酵素が存在しており、プロトン(H+)を膜間腔へ汲み出す。この過程は非常に効率的だが、不十分な反応により活性酸素種を生じてしまうことがある(活性酸素#活性酸素と人体の関係参照のこと)。これがいわゆる酸化ストレスで、ミトコンドリアの機能低下や老化に関与していると考えられている[15]。
グルコーストランスポーターであるGLUT1を介してデヒドロアスコルビン酸がミトコンドリアに輸送され、その後ビタミンCに還元され、活性酸素によるフリーラジカルの大部分が生成される場所であるミトコンドリアに蓄積される。アスコルビン酸(ビタミンC)は、ミトコンドリアのゲノムと膜を保護する[16]。
プロトンが膜間腔へ汲み出されることにより、内膜の内外でプロトン濃度の差(電気化学的勾配)が生じる。汲み出されたプロトンはATP合成酵素を通じてマトリックスへ戻ることができ、このときにそのポテンシャルを使ってADPと無機リン酸(Pi)からATPを生成する。生成されたATPはATP/ADPトランスポーターによりミトコンドリアから細胞質へ輸送され細胞の活動エネルギー源となる[12]。
この原理を化学浸透説とよび、ピーター・ミッチェルが最初に唱えその功績によって1978年にノーベル化学賞を受賞した[17][18]。ATP合成酵素の反応機構を明らかにしたポール・ボイヤーとジョン・E・ウォーカーには1997年にノーベル化学賞を授与された[19]。
脂肪酸の輸送とβ酸化
ミトコンドリアにおける脂肪酸の輸送についてはβ酸化#脂肪酸の動員及びβ酸化#脂肪酸の活性化とミトコンドリア内への輸送を参照のこと。ミトコンドリアにおけるβ酸化についてはβ酸化#β酸化反応および酵素群を参照のこと。ミトコンドリアのマトリックスで生成されたアセチルCoAは上述のようにクエン酸回路でエネルギーに変換される。
筋肉とミトコンドリア
速筋線維はミトコンドリアが少なく、グリコーゲンが比較的多いので白く見え、糖分解により乳酸ができやすい。乳酸性閾値から上の運動強度では速筋線維が多く使われるようになる。遅筋線維や心筋はミトコンドリアが多いので赤く見え、乳酸を作るよりは乳酸を外から取り込んでエネルギー源として使っている。運動強度が低い場合は遅筋線維が主として働いている。つまり速筋線維のグリコーゲンが乳酸を介して遅筋線維や心筋のミトコンドリアで使われている。このように乳酸の代謝では細胞膜を通過して他の細胞に乳酸が輸送される必要がある。この乳酸の輸送は乳酸だけではなくピルビン酸などの輸送にも関わることからモノカルボン酸の輸送担体(Monocarboxylate Transporter (MCT))と呼ばれている[20]。
熱産生
ある条件下では、膜間腔のプロトンはATP合成に関与することなく、促進拡散によってマトリックスに戻ることがある。これは「プロトンのリーク」とか「ミトコンドリアの脱共役」と呼ばれ、蓄積されていた電気化学ポテンシャルは熱として解放されることになる。thermogeninをはじめとする一群のプロトンチャネル(脱共役タンパク質)が媒介しており、非ふるえ熱産生に関わっている[21]。Thermogeninは若齢や冬眠中の哺乳類に見られる褐色脂肪組織のミトコンドリアに存在している。
アポトーシス
DNA損傷などのストレスは、アポトーシス誘導分子p53やアポトーシスを調節するBcl-2ファミリータンパク質を介して、ミトコンドリアの膜電位を変化させ、その結果、ミトコンドリアからシトクロムcが漏出し、アポトーシスへとつながる[22]。シトクロムcは、細胞質に存在するApaf-1やカスパーゼ-9と結合して、アポトソーム(apoptosome)と呼ばれる集合体を形成する。これによって活性化されたカスパーゼ-9が、下流のエフェクターを活性化していく。
カルシウム貯蔵
細胞中のカルシウム濃度は様々な機構によって制御されており、細胞中の情報伝達に重要な役割を果たしている。ミトコンドリアは一過的なカルシウム貯蔵能があり、細胞におけるカルシウム濃度の恒常性に貢献している[23]。ミトコンドリアは迅速にカルシウムを取り込むことができ、それを後々放出することで、カルシウム濃度の緩衝作用を果たしている[24][25][26]。カルシウムの貯蔵場所としては小胞体が最も顕著であり、この点に関して小胞体とミトコンドリアは協調している[27]。
カルシウムは内膜になるカルシウム輸送体によりマトリックスへ取り込まれる[28]。これはミトコンドリアの膜電位に依存している[23]。
逆にカルシウムの放出は、ナトリウム・カルシウム対向輸送か、もしくはカルシウム依存性カルシウム放出系によって行われる[28]。これによってセカンドメッセンジャー系が起動され、神経伝達物質やホルモンの放出が行われる。
ミトコンドリアゲノム
ミトコンドリア中にはDNAが存在しており、ここに細胞核のものとは異なる独自の遺伝情報を持っている。通常はGC含量が低く(20-40%)、基本的なゲノムのサイズは数十kb程度のDNAであり、電子伝達系に関わるタンパク質、リボソームRNAやtRNAなど数十種類の遺伝子がある。しかしDNA分子の大きさや形状、コードされている遺伝子の数や種類などは、生物によって大きく異なる。ヒトを含む脊椎動物のmtDNAは真核生物の中ではかなり特殊な性質を多く持っており、研究はよく進んでいるものの安易な一般化は慎まなければならない。
最も小さなmtDNAを持つ生物はアピコンプレックス門の原虫で、大きさわずか6 kbの線状ゲノムである。電子伝達系に関わる3つのタンパク質遺伝子と、断片化されたリボソームRNA遺伝子群のみが存在している。逆に最も大きなmtDNAは、マスクメロンのもつ2400kbという巨大なゲノムである。ただし遺伝子数は比較的多いものの100弱に過ぎず、大量の反復配列やグループ2イントロンなどの非遺伝子領域が大部分を占める。ヒトを含む多細胞動物のmtDNAはいずれも比較的似通っており、大きさ16 kb前後の単一の環状DNAで構成されている。遺伝子は37あり、その内訳は、呼吸鎖複合体とATP合成酵素のサブユニットが13、tRNAが22、rRNAが2となっている。
遺伝子地図などではmtDNAが環状に表現されることが多い。しかし物理的に環状のmtDNAを持つ生物はごく一部に限られ、多くの生物では環状の基本構造からトイレットペーパーを引き出すかのように連続的に複製されており、その結果mtDNAの大部分は基本単位が何度も繰り返す線状反復構造になっている。また少数派ではあるが、常に線状のミトコンドリアを持つ生物も存在している。
遺伝子
ミトコンドリアゲノムはαプロテオバクテリアから受け継がれたものであり、その遺伝子発現は細菌と共通した特徴を持っている。複数の遺伝子がまとめて転写され、それが遺伝子ごとに切断されポリアデニル化されて成熟mRNAとなること、翻訳の開始にフォルミル化メチオニンが利用されること、細胞核に存在するようなスプライソソーム型のイントロンが存在しないこと、などが挙げられる。
ミトコンドリアの遺伝暗号表は、細胞核や一般の原核生物で利用されている普遍暗号表と比べて若干の差がある。顕著な例として通常では終止コドンであるはずのUGAがトリプトファンをコードしている場合が多いことが挙げられるが、例外も多く様々な生物で少しずつ異なる暗号表を用いているというのが実態である[29]。 またミトコンドリアではしばしばRNA編集が行われる。たとえば高等植物のミトコンドリアでは、DNA配列上のCGGがmRNAではUGGと編集されてトリプトファンをコードするという例が知られている[30]。
ミトコンドリアの機能に関わる全ての遺伝子がミトコンドリアゲノムに存在しているわけではない。ミトコンドリアゲノムは細菌のゲノムと比べると遺伝子数が極端に減少しており、一方で大多数の遺伝子は細胞核にコードされ遺伝子産物がミトコンドリアへと輸送される。これは進化の過程で遺伝子が細胞核へ移動したからだと考えられている。こうした現象は比較的よくあった出来事だと考えられ、マイトソームなどのように全てのDNAを完全に失ったようなミトコンドリアも存在している。一方、原生生物のレクリノモナス(Reclinomonas americana)は、他の生物では細胞核から輸送されているようなタンパク質がmtDNAに存在しており、比較的原始的なミトコンドリアゲノムを未だに保っていると考えられている。
ミトコンドリアには呼吸機能に関与する疎水性のタンパク質があり、これらをミトコンドリアの内部で作らざるを得ないのがミトコンドリアに遺伝子が残っている理由の一つとなっている[31]。
異数性
1つのミトコンドリアには2〜10コピーのDNA分子が存在する[32]。その全てが完全に同じ情報を持つわけではなく、複数の異質のDNA分子を含んでいることが確認されている[8]。
起源
ミトコンドリアは好気性細菌でリケッチアに近いαプロテオバクテリアが真核細胞に共生することによって獲得されたと考えられている[8]。リン・マーギュリスの細胞内共生説では単に好気性バクテリアが起源とされていたが、その後すぐの1970年代にすでにミトコンドリアの起源が現在でいうαプロテオバクテリアだという意見が出ている。脱窒細菌Paracoccus denitrificansや暗所好気条件で培養した紅色光合成細菌Rhodobacter sphaeroidesは呼吸鎖の構成や阻害剤への応答がミトコンドリアのものと類似しており、特にシトクロムcがミトコンドリアのものと互換性を持つ点が注目された[33]。
細胞核DNAにコードされているシトクロムcだけでなく、mtDNAにコードされているリボソームRNAの配列を使った系統解析でもαプロテオバクテリア起源であることが示され、1980年代にはミトコンドリアのαプロテオバクテリア起源は受け入れられるようになった[34]。
ただし初期の解析では、高等植物ミトコンドリアのリボソームRNAの配列が他のミトコンドリアの配列と比べて進化的距離が非常に小さかったため、ミトコンドリアの起源は単独ではなく、高等植物のミトコンドリアは新たに獲得されたものだという意見もあった[34]。こうした意見は現在では否定され、真核生物のミトコンドリアの起源は単一であるとされている[35]。
αプロテオバクテリアは非常に多様な細菌を含む分類群であり、その中でどのような細菌がミトコンドリアの起源となったかについては長く議論が続いている。初期には前述の通り脱窒細菌や光合成細菌が起源だと考えられていたが、シャペロニンHsp60(GroEL)を用いた系統解析によりリケッチアが最も近縁であると示されてからは、これが有力説となった。リケッチアは、細胞内寄生体であること、TCA回路を持ち好気呼吸ができるが解糖系を持たないこと、細胞膜にADP/ATP輸送体を持っていること、ゲノムが小さくAT含量が高いことなど、ミトコンドリアと共通した特徴を持っている[35]。
1998年に発疹チフスリケッチア(Rickettsia prowazekii)のゲノムが解読され、祖先的とされるReclinomonas americanaのミトコンドリアゲノムと共通している遺伝子や、配置順が保存された遺伝子群などが見出され解析されている。その多くはミトコンドリアがリケッチアに近縁であるという仮説を支持するものであったが、ADP/ATP輸送体については予想に反して起源を異にしていることが示されている[36]。
20世紀末から21世紀初頭にかけて、世界中の海洋には自由生活性で浮遊性の細菌ペラジバクター(暫定的にCandidatus Pelagibacter ubiqueと命名されている)が存在していることが明らかとなった[37]。
ペラジバクターはリケッチア目の中でも最も祖先的な位置から派生する生物であり、ミトコンドリアの起源をペラジバクターとその他一般的なリケッチアとの間に求めることができる[38]。
アメーバに似た原生生物であるペロミクサや微胞子虫など、いくつかの原生生物はミトコンドリアを持っていない。これを、ミトコンドリアが共生する以前の真核生物の生き残りと見る説があった(→アーケゾア仮説)が、後に否定されている。
生物の系統との関係
上記のようなミトコンドリアの特徴は、動物、植物、菌類にほぼ共通であるが、それ以外の原生動物では、若干異なった形のものがある。特にクリステの形についてははっきりと異なったものがある。一般のミトコンドリアでは内膜がひだのように折れ曲がり、クリステは平坦な板のような形をしている。しかし、粘菌類の場合、クリステは内膜から内部へと放射状に入り込む管の形で、管の表面にATP合成酵素の手段が並んでいる。また、内部の中央にDNAを含んだ塊があって、ミトコンドリア核と呼ばれる。このような、管状のクリステを持つミトコンドリアは、繊毛虫やアピコンプレックス類、アメーバ類、クロララクニオン藻類などの原生生物からも知られる。
また、ミドリムシ類とトリパノソーマでは、クリステは団扇型になっていることも知られている。これらのミトコンドリアは、細長くて枝分かれをして、細胞内に広がっている。トリパノソーマでは、鞭毛の基部にキネトプラストと呼ばれる袋状の構造が知られており、その中の顆粒にはDNAが含まれているが、これはミトコンドリアの一部である。
がんとミトコンドリア
1955年、オットー・ワールブルクは、体細胞が長期間低酸素状態に晒されると呼吸障害を引き起こし、通常酸素濃度環境下に戻しても大半の細胞が変性や壊死を起こし、ごく一部の細胞が酸素呼吸に代わるエネルギー生成経路を昂進させて生存する細胞が癌細胞となる説を発表した。酸素呼吸よりも発酵(=解糖系)によるエネルギー産生に依存するものは下等動物や胎生期の未熟な細胞が一般的であり、体細胞が酸素呼吸によらず発酵に依存することで細胞が退化し癌細胞が発生するとしている[39]。
がんの発生とmtDNAの突然変異の関与は古くから指摘されてきた。その理由は特定の発がん性化学物質がDNAよりもmtDNAに結合しやすいこと、がん組織のmtDNAは正常組織よりも高い割合で突然変異が蓄積していたことが観察されたことによる。しかし、母性遺伝するがんの存在が確認されていないことや、DNAの影響を排除しmtDNA単独でのがんへの影響を検証する手法が確立されていないなどが証明の障害になっていた。ところで、2008年筑波大学の林純一らが、がんの転移能獲得という悪性化にミトコンドリアが関与している[40]ことを、マウス肺がん細胞の細胞質移植による細胞雑種の比較により、mtDNAの特殊な病原性突然変異によってがん細胞の転移能獲得の原因になることを発見し、ヒトのがん細胞株でもmtDNAの突然変異ががん細胞の転移能を誘導しえることをあきらかにし、すくなくともmtDNAがATP合成以外の生命現象にも関与するとを明らかにした。また、林らによるとmtDNAの突然変異には活性酸素種(ROS)の介在が重要であり、ROSを除去すれば転移能の抑制が可能ではないかとしている。がんの転移能の獲得メカニズムは複雑であり、様々な要因が考えられるのでこれはその要因の一つにすぎない。
「ミトコンドリア・イブ」
ミトコンドリアのDNAは母親のmtDNAを引き継ぐ(同種交配の場合卵子に入った精子のミトコンドリアが選択的に排除されてしまうから)ことを根拠に、現生人類の起源の地が探られた。世界中に分布するヒトからmtDNAを調べて現在の分布地図から現生人類の起源とその移動について推察する作業から、大昔のアフリカのある女性が今の人類の全てのミトコンドリアについての「母親」であるとの仮説が発表された。なお、その他の遺伝情報についてすべてこの女性に由来するということではないし、むろん全人類の起源が一人の女性にあるわけでもない。この女性はキリスト教徒の宗教的説話から「ミトコンドリア・イブ」と呼ばれている。なお、実験的に異種交配させた受精卵では、精子由来のミトコンドリアを排除するプロセスが失敗する場合がある。
フィクション
小説
1995年に第2回日本ホラー小説大賞を受賞した瀬名秀明の『パラサイト・イヴ』は、ミトコンドリアの共生起源説、および、人類進化におけるミトコンドリア・イブ説 (Wikipedia英語版Mitochondrial Eve参照) に基づき、現在のミトコンドリアは細胞の支配下にあるが、もしもそれが反乱を起こしたならば、という仮定の物語で話題を呼び、映画やゲーム化も行なわれた。
脚注
- ↑ 林純一「ミトコンドリアDNAに突然変異をもつ細胞は自然免疫により排除されることを発見」筑波大学生命科学研究科発表 「Journal of Experimental Medicine」電子版 2011.Oct.12
- ↑ ニック・レーン、斉藤隆央訳、2007年、「ミトコンドリアが進化を決めた」p1、P16、みすず書房、ISBN 978-4-622-07340-6
- ↑ Herrmann JM, Neupert W (2000 April). “Protein transport into mitochondria”. Curr Opin Microbiol 3 (2): 210–214. doi:10.1016/S1369-5274(00)00077-1. PMID 10744987.
- ↑ Hayashi T, Rizzuto R, Hajnoczky G, Su TP (February 2009). “MAM: more than just a housekeeper”. Trends Cell Biol. 19 (2): 81–8. doi:10.1016/j.tcb.2008.12.002. PMC 2750097. PMID 19144519.
- ↑ Chipuk JE, Bouchier-Hayes L, Green DR (2006). “Mitochondrial outer membrane permeabilization during apoptosis: the innocent bystander scenario”. Cell Death and Differentiation. 13 (8): 1396–1402. doi:10.1038/sj.cdd.4401963. PMID 16710362.
- ↑ http://www10.showa-u.ac.jp/~biolchem/H20-P2cell-11.pdf
- ↑ Mannella CA (2006). “Structure and dynamics of the mitochondrial inner membrane cristae”. Biochimica et biophysica acta 1763 (5–6): 542–548. doi:10.1016/j.bbamcr.2006.04.006. PMID 16730811.
- ↑ 8.0 8.1 8.2 8.3 黒岩常祥著 『ミトコンドリアはどこからきたか』 日本放送出版 2000年6月30日第1刷発行 ISBN 4140018879
- ↑ Stoimenova M, Igamberdiev AU, Gupta KJ, Hill RD (July 2007). “Nitrite-driven anaerobic ATP synthesis in barley and rice root mitochondria”. Planta 226 (2): 465–74. doi:10.1007/s00425-007-0496-0. PMID 17333252.
- ↑ TCA回路 講義資料のページ
- ↑ Monty Krieger; Matthew P Scott; Matsudaira, Paul T.; Lodish, Harvey F.; Darnell, James E.; Lawrence Zipursky; Kaiser, Chris; Arnold Berk. Molecular Cell Biology, Fifth Edition. San Francisco: W. H. Freeman. ISBN 0-7167-4366-3.
- ↑ 12.0 12.1 真島 英司、寺田 弘、「ATPはいかにして膜を透過するか:ループの協調的スウィングによるミトコンドリアADP/ATPキャリアーの機能発現」、『生物物理』Vol. 38 (1998) No. 6、P 245-249
- ↑ 第5回 5.エネルギーの生産-サイトゾールとミトコンドリア 更新日:2002/04/08 教養部生物学の資料[1]
- ↑ “Citric acid cycle.”, In: Biochemistry., Fourth, New York: W.H. Freeman and Company, 509–527, 569–579, 614–616, 638–641, 732–735, 739–748, 770–773. ISBN 0 7167 2009 4.
- ↑ Huang, K.; K. G. Manton (2004). “The role of oxidative damage in mitochondria during aging: A review”. Frontiers in Bioscience 9: 1100–1117. doi:10.2741/1298. PMID 14977532.
- ↑ KC S, Carcamo JM, Golde DW (2005). “Vitamin C enters mitochondria via facilitative glucose transporter 1 (Glut1) and confers mitochondrial protection against oxidative injury”. FASEB J 19 (12): 1657–67. doi:10.1096/fj.05-4107com. PMID 16195374.
- ↑ Mitchell P, Moyle J (1967-01-14). “Chemiosmotic hypothesis of oxidative phosphorylation”. Nature. 213 (5072): 137–9. doi:10.1038/213137a0. PMID 4291593.
- ↑ Mitchell P (1967-06-24). “Proton current flow in mitochondrial systems”. Nature. 25 (5095): 1327–8. doi:10.1038/2141327a0. PMID 6056845.
- ↑ Nobel Foundation. “Chemistry 1997”. . 2007閲覧.
- ↑ 新たな乳酸の見方、八田 秀雄、学術の動向、Vol. 11 (2006) No. 10
- ↑ Mozo J, Emre Y, Bouillaud F, Ricquier D, Criscuolo F (2005 November). “Thermoregulation: What Role for UCPs in Mammals and Birds?”. Bioscience Reports. 25 (3-4): 227–249. doi:10.1007/s10540-005-2887-4. PMID 16283555.
- ↑ アポトーシスの分子機構 太田成男、石橋佳朋「脳と発達」Vol.31(1999)No.2
- ↑ 23.0 23.1 Editor-in-chief, George J. Siegel; editors, Bernard W. Agranoff... [et al.]; illustrations by Lorie M. Gavulic (1999). in Siegel GJ, Agranoff BW, Fisher SK, Albers RW, Uhler MD: Basic Neurochemistry, 6, Lippincott Williams & Wilkins. ISBN 0-397-51820-X.
- ↑ Rossier MF (2006). “T channels and steroid biosynthesis: in search of a link with mitochondria”. Cell Calcium. 40 (2): 155–64. doi:10.1016/j.ceca.2006.04.020. PMID 16759697.
- ↑ Brighton, Carl T. and Robert M. Hunt (1974): "Mitochondrial calcium and its role in calcification", Clinical Orthopaedics and Related Research 100: 406-416
- ↑ Brighton, Carl T. and Robert M. Hunt (1978): "The role of mitochondria in growth plate calcification as demonstrated in a rachitic model", Journal of Bone and Joint Surgery, 60-A: 630-639
- ↑ Pizzo P, Pozzan T (2007 October). “Mitochondria–endoplasmic reticulum choreography: structure and signaling dynamics”. Trends Cell Bio. 17 (10): 511–517. doi:10.1016/j.tcb.2007.07.011. PMID 17851078.
- ↑ 28.0 28.1 Miller RJ (1998). “Mitochondria – the kraken wakes!”. Trends in Neurosci. 21 (3): 95–97 doi=10.1016/S0166–2236(97)01206–X. doi:10.1016/S0166-2236(97)01206-X.
- ↑ Jukes TH, Osawa S (1990-12-01). “The genetic code in mitochondria and chloroplasts”. Experientia. 46 (11–12): 1117–26. doi:10.1007/BF01936921. PMID 2253709.
- ↑ Hiesel R, Wissinger B, Schuster W, Brennicke A (2006). “RNA editing in plant mitochondria”. Science. 246 (4937): 1632–4. doi:10.1126/science.2480644. PMID 2480644.
- ↑ 池田清彦、『不思議な生き物-生命38億年の歴史と謎』203p、2013年4月25日、角川学芸出版、ISBN 978-4-04-653275-6
- ↑ Wiesner RJ, Ruegg JC, Morano I (1992). “Counting target molecules by exponential polymerase chain reaction, copy number of mitochondrial DNA in rat tissues”. Biochim Biophys Acta 183 (2): 553–559. PMID 1550563.
- ↑ John P, Whatley FR. (1975). “Paracoccus denitrificans and the evolutionary origin of the mitochondrion.”. Nature 254 (5500): 495-498. PMID 235742.
- ↑ 34.0 34.1 Yang D, Oyaizu Y, Oyaizu H, Olsen GJ, Woese CR. (1985). “Mitochondrial origins”. Proc Natl Acad Sci 82 (13): 4443-4447. PMID 3892535.
- ↑ 35.0 35.1 Viale AM, Arakaki AK. (1994). “The chaperone connection to the origins of the eukaryotic organelles.”. FEBS Lett. 341 (2-3): 146-151. PMID 7907991.
- ↑ Andersson SG, Zomorodipour A, Andersson JO, Sicheritz-Pontén T, Alsmark UC, Podowski RM, Näslund AK, Eriksson AS, Winkler HH, Kurland CG. (1998). “The genome sequence of Rickettsia prowazekii and the origin of mitochondria.”. Nature 396 (6707): 133-140. PMID 9823893.
- ↑ Rappe et al. (2002). “Cultivation of the ubiquitous SAR11 marine bacterioplankton clade”. Nature 418 (6898): 630-633. PMID 12167859.
- ↑ Williams KP, Sobral BW, Dickerman AW. (2007). “A robust species tree for the alphaproteobacteria.”. J Bacteriol. 189 (13): 4578-4586. PMID 17483224.
- ↑ Warburgの「癌細胞の起原」に就いて、小野 興作, 大島 福造, 渡辺 漸, 八木 日出雄, 津田 誠次, 陣内 伝之助, 平木 潔, 妹尾 左知丸, 浜崎 幸雄、岡山医学会雑誌、Vol. 70 (1958) No. 12supplement
- ↑ Hayashi, J., et. al. (2008). “ROS-generating mitochondrial DNA mutations can regulate tumor cell metastasis”. Science 320 (5876): 661-664. PMID 18388260.